复百澳(苏州)生物医药科技有限公司
9 年
手机商铺
商家活跃:
产品热度:
- NaN
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
- 3.7
文献支持
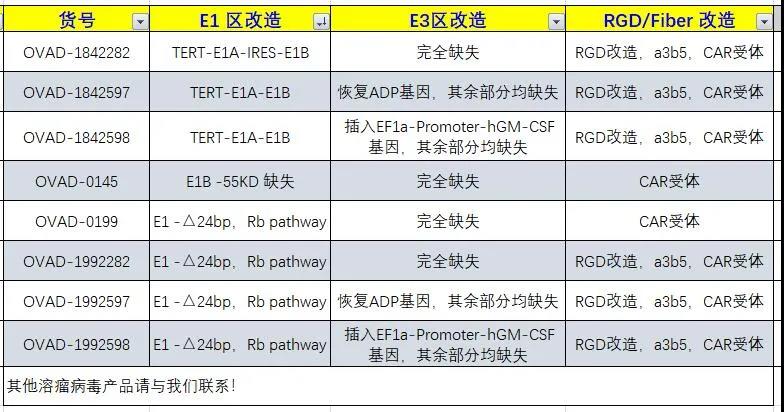
溶瘤腺病毒改造服务(OVAD184)
询价
推荐产品
公司新闻/正文
溶瘤腺病毒活化树突细胞提升免疫治疗效果
1345 人阅读发布时间:2021-01-28 20:03

(图片来源:https://doi.org/10.1089/hum.2020.222)
研究者首先使用 Ad3-WT,Ad3-hTERT-E1A 及 Ad3-hTERT-CMVhCD40L 三种溶瘤病毒感染前列腺癌细胞 PC-3和 PC-3MM2 细胞进行体外杀伤实验,结果显示三种溶瘤病毒均能有效的对肿瘤细胞进行杀伤,三者之间杀伤效果无显著性差异。
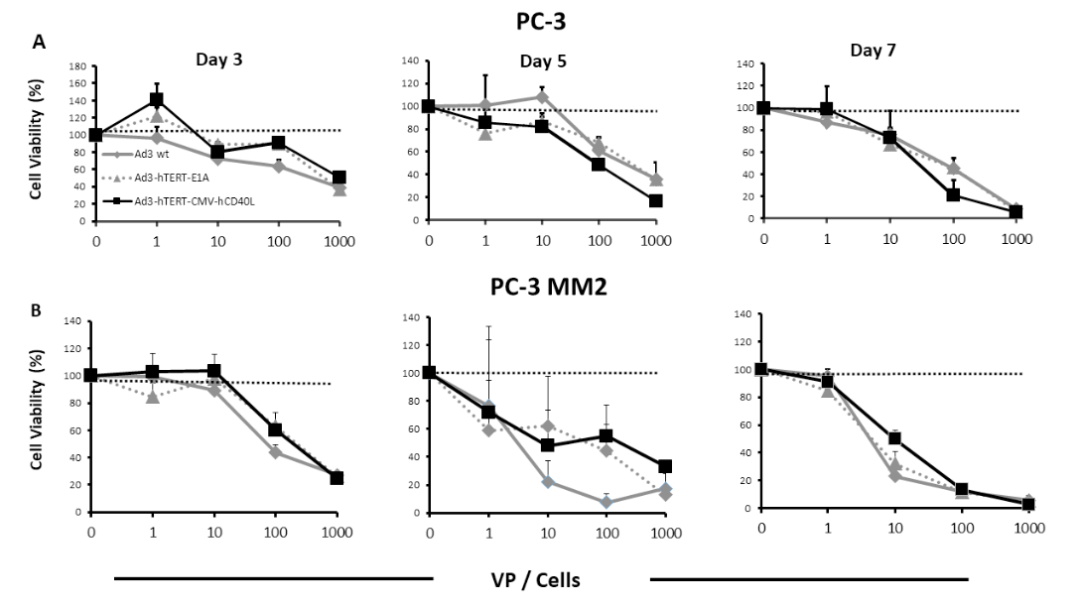
(图片来源:https://doi.org/10.1089/hum.2020.222)
进一步实验,研究者将 PC3-MM2 肿瘤细胞皮下植入免疫缺陷 SCID 小鼠中。14 天后开始治疗实验,治疗的第 0 天,给小鼠静脉注射 1×10^6 PBMC 进行人源化处理。然后在第 1,3,5 天,分别瘤内注射溶瘤病毒 Ad3-hTERT-E1A及Ad3-hTERT-CMVhCD40L ,剂量为 1×10^8 VP/ 次。随后,对肿瘤的体积和生存率进行统计分析,和对照组及 PBMC 单独治疗组相比,联合治疗组的治疗效果有显著性差异。
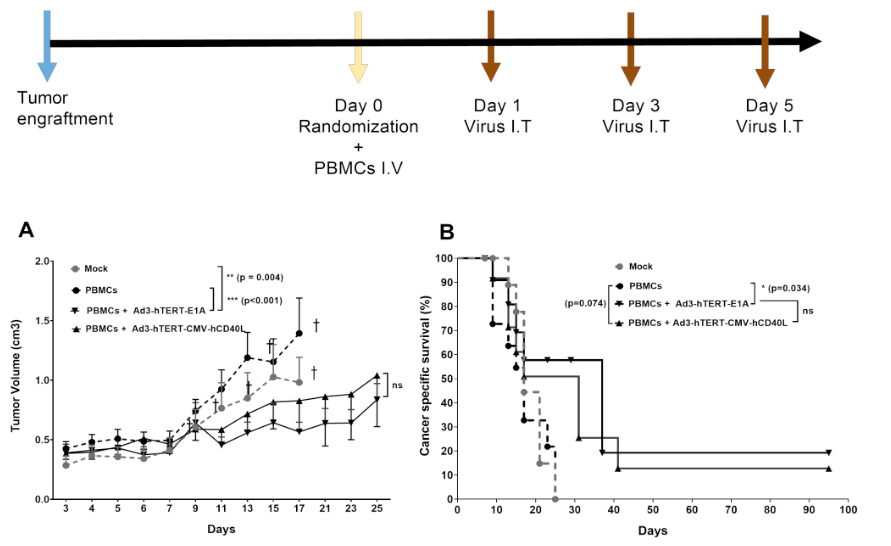
(图片来源:https://doi.org/10.1089/hum.2020.222)
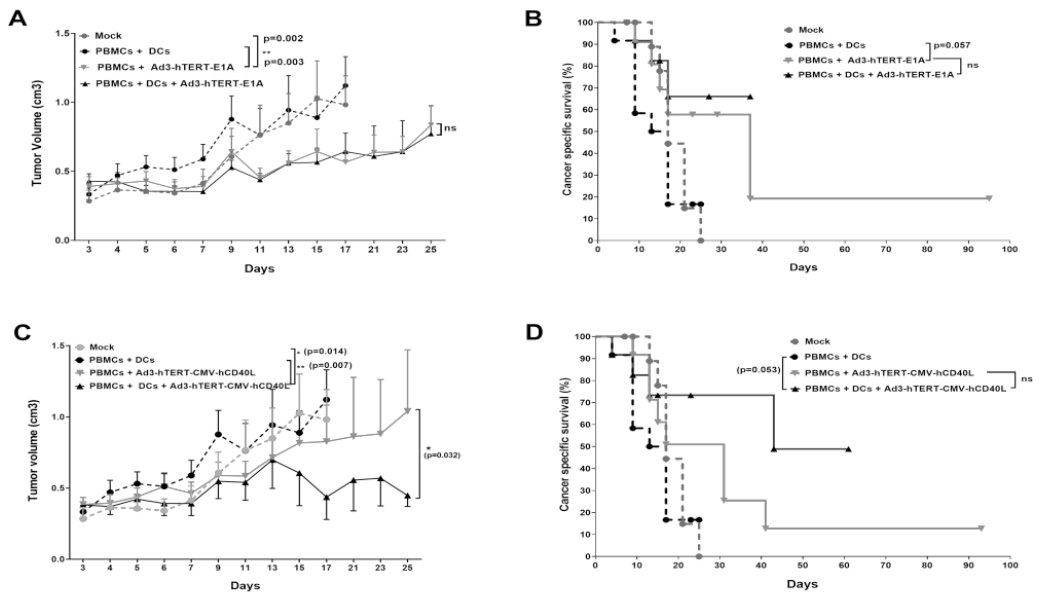
(图片来源:https://doi.org/10.1089/hum.2020.222)
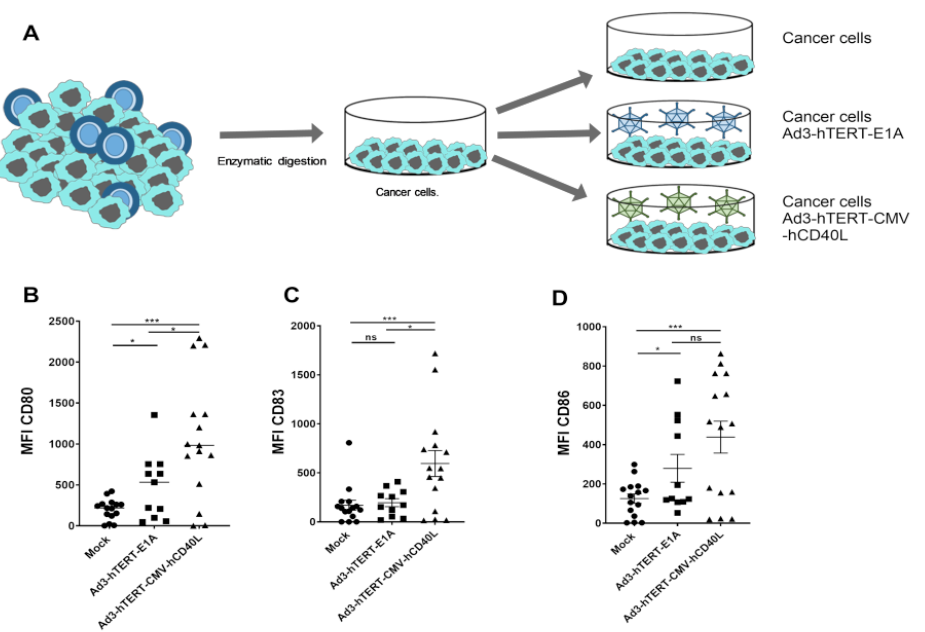
(图片来源:https://doi.org/10.1089/hum.2020.222)
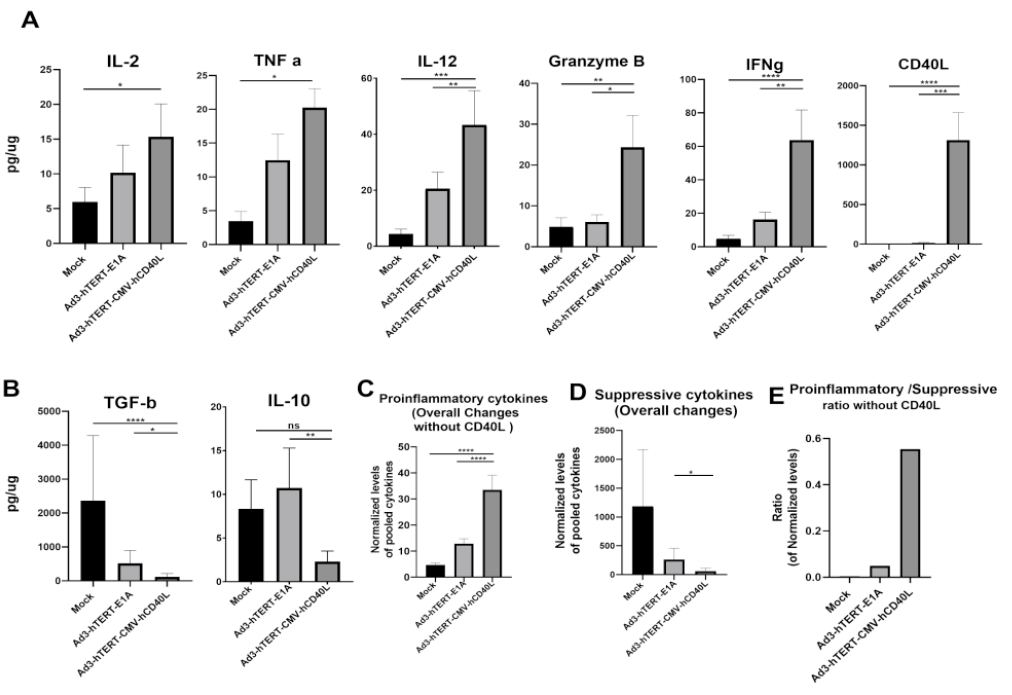
(图片来源:https://doi.org/10.1089/hum.2020.222)
综合分析,溶瘤腺病毒(Ad3-hTERT-CMV-hCD40L;),通过表达 CD40L 刺激前列腺肿瘤微环境中的树突细胞(DC)活化,并明显增加促炎细胞因子的释放,进一步激活细胞毒性T细胞,从而产生治疗性免疫反应,这为该溶瘤腺病毒的下一步的临床实验的开展,奠定基础并提供了理论依据。
补充:
参考文献:
https://doi.org/10.1089/hum.2020.222
溶瘤病毒现货产品