复百澳(苏州)生物医药科技有限公司
9 年
手机商铺
- NaN
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
- 3.7
推荐产品
公司新闻/正文
新冠病毒入侵及传染性研究取得重要进展
1943 人阅读发布时间:2021-02-25 18:39
近日,复旦大学基础医学院张荣/袁正宏/蔡启良等在 Nature Communications 上发表了题为 A genome-wide CRISPR screen identifies host factorsthat regulate SARS-CoV-2 entry 的研究论文。该文在去年 8 月提交到预印版 BioRxiv上,题为 The S1/S2 boundary of SARS-CoV-2 spike proteinmodulates cell entry pathways and transmission。
该研究发现新冠病毒 S 蛋白多碱性氨基酸的插入可以调控病毒的入胞途径,该位点的缺失驱使病毒入胞途径从膜融合向内体入胞的转变。同时,利用缺失突变株进行全基因组 CRISPR 筛选,鉴定发现一系列调控病毒内吞途径以及病毒受体 ACE2 细胞膜表达相关的宿主因子。该研究还在仓鼠模型中进一步揭示 S 蛋白碱性氨基酸的插入与病毒的传染性密切相关。

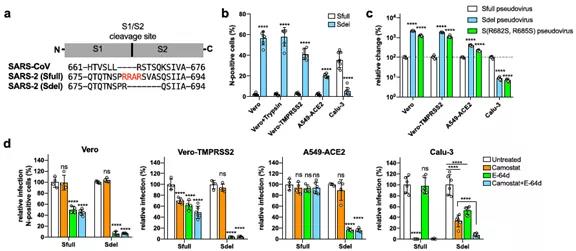
图 1:新冠病毒 S 蛋白多碱性氨基酸缺失改变病毒的入胞途径
为了深入揭示新冠病毒内体入胞途径的调控机制,作者利用获得的多碱性氨基酸缺失突变病毒在 A549-ACE2 细胞上进行全基因组 CRISPR 筛选,鉴定发现一系列与货物转运相关的复合体如 Retromer、CCC、WASH、Arp 2 / 3 等,以及其它胆固醇转运相关基因如 NPC1 和 NPC2 等宿主因子( 图 2 )。
进一步验证显示,这些因子对经内体入胞的 SARS-CoV-2 缺失突变体至关重要,而对野生型病毒作用不明显,特别是敲除 CTSL 基因对野生型无影响。此外,研究还证明这些因子对 SARS-CoV 和 MERS-CoV 的入胞都至关重要,是一类冠状病毒通用的内体入胞途径相关的宿主因子。此外,该研究还发现一类可以调控 ACE2 的细胞膜定位表达的宿主因子。
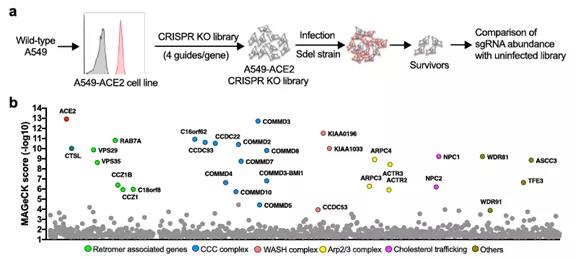
图 2 :全基因组 CRISPR 筛选发现 SARS-CoV-2、SARS-CoV 和 MERS-CoV 通用的内体入胞相关宿主因子
为进一步的揭示 S 蛋白碱性氨基酸插入对病毒感染的影响,作者建立了新冠感染仓鼠模型( goldenSyrian hamster )。新冠病毒可以自然高效的通过呼吸道感染野生型仓鼠,是良好的小动物模型。作者系统的评价了碱性氨基酸的缺失在不同组织器官如鼻腔上皮、气管、肺、脑、心、肠、脾、肝、肾脏等的感染特性,结果显示缺失突变病毒在不同器官组织以及粪便中表现出较低的病毒载量和较轻病症。更重要的是,通过接触传染性试验证明,缺失突变病毒的传染性几乎丧失,在与感染仓鼠接触的仓鼠鼻腔上皮和肺组织中检测不到活病毒存在,这表明了 S 1 / S 2 附近的多碱基序列在传播中发挥的关键作用。这很大可能是由于野生型病毒使用了更有效的质膜融合入胞途径( 图 3 )。
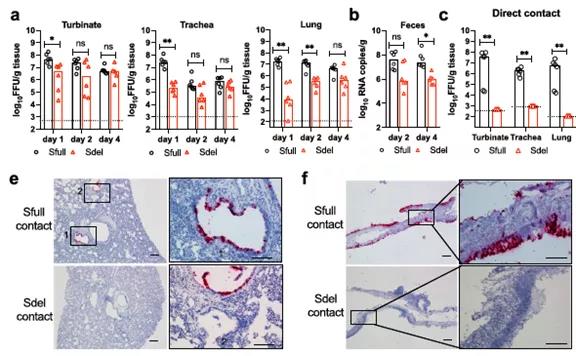
图 3 :新冠病毒S蛋白碱性氨基酸的插入与传染性相关
综上所述,该研究比较系统的揭示了新冠病毒 S 蛋白碱性氨基酸的插入对病毒入胞途径以及传染性的影响,并用S蛋白缺失突变病毒鉴定发现了一些列可调控病毒入胞的宿主基因,特别是调节内体入胞途径相关的基因( 图 4 )。
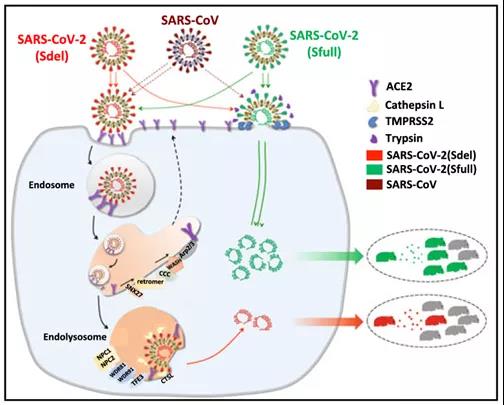
图 4:新冠病毒 S 蛋白碱性氨基酸的插入调控病毒入胞途径及传染性
新冠病毒知识补充
新冠病毒(SARS-CoV- 2)和非典病毒(SARS-CoV)的核苷酸序列具有近 80% 同源性,均使用相同细胞受体血管紧张素转换酶 2(ACE2)进入靶细胞。但新发的 SARS-CoV- 2 似乎具有更强的传染性。新冠病毒编码的刺突蛋白(S)在决定入胞、宿主嗜性、免疫原性和致病性等方面起着至关重要的作用。
SARS-CoV- 2 刺突蛋白与其他蝙蝠来源的类 SARS-CoV 病毒的 S 蛋白之间存在一个显著差异,即在 S1 和 S2 亚基的切割位点交界处插入了多个碱基氨基酸(RRAR),在蛋白翻译后转运过程中可以被位于高尔基体的弗林酶(Furin)切割,可能预先激活 S 蛋白,降低 SARS-CoV- 2 对位于细胞质膜上的蛋白酶如跨膜丝氨酸蛋白酶 2(TMPRSS2)的依赖性,促进病毒的入胞。
研究表明多碱性氨基酸的插入可以促进细胞间的膜融合,表达缺失了「RRAR」氨基酸序列的 SARS-CoV- 2 S 蛋白引发的细胞膜融合程度显著降低。也有研究发现,多碱性氨基酸的插入在发生切割后,会形成「RRAR」即所谓的 C-end rule ( CendR ),可以被 Neuropilin- 1 ( NRP 1 ) 识别,有助于病毒的感染入侵。值得注意的是,S 蛋白的 S1 和 S2 亚基切割位点附近的序列似乎是不稳的,在细胞培养和患者样品中均检测到了不同程度的缺失突发生。
冠状病毒的入胞通常有两种途径:病毒颗粒与质膜融合(早期入胞途径)和与内体融合(晚期入胞途径)。相较于内体融合途径,病毒直接与细胞质膜融合通路更高效快捷。位于细胞质膜的 TMPRSS2 或者外源蛋白酶的存在如胰酶等,会触发质膜融合途径。否则,它将通入晚期途径内吞进入细胞。内体的低 pH 环境会激活组织蛋白酶 L(CTSL),触发病毒囊膜与内体的膜融合从而释放病毒基因组。
研究表明,在高表达 TMPRSS2 但低表达 CTSL 的 Calu- 3 人肺细胞中,SARS-CoV 更倾向于通过早期膜融合途径进入细胞。针对新冠病毒 S 蛋白插入的多碱性氨基酸的功能是研究热点。此外,调控新冠病毒入侵途径相关的宿主因子鉴定发现也值得深入挖掘。
原文链接:
https://www.nature.com/articles/s41467 - 021 - 21213 - 4?utm_source = other&utm_medium = other&utm_content = null&utm_campaign = JRCN_1_LW01_CN_natureOA_article_paid_XMOL
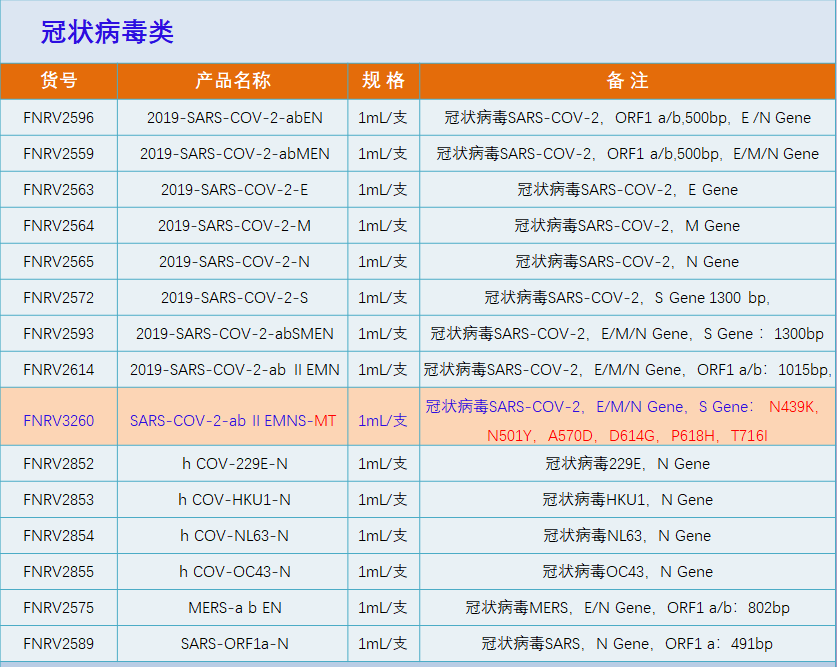
抗体中和实验及机制研究产品
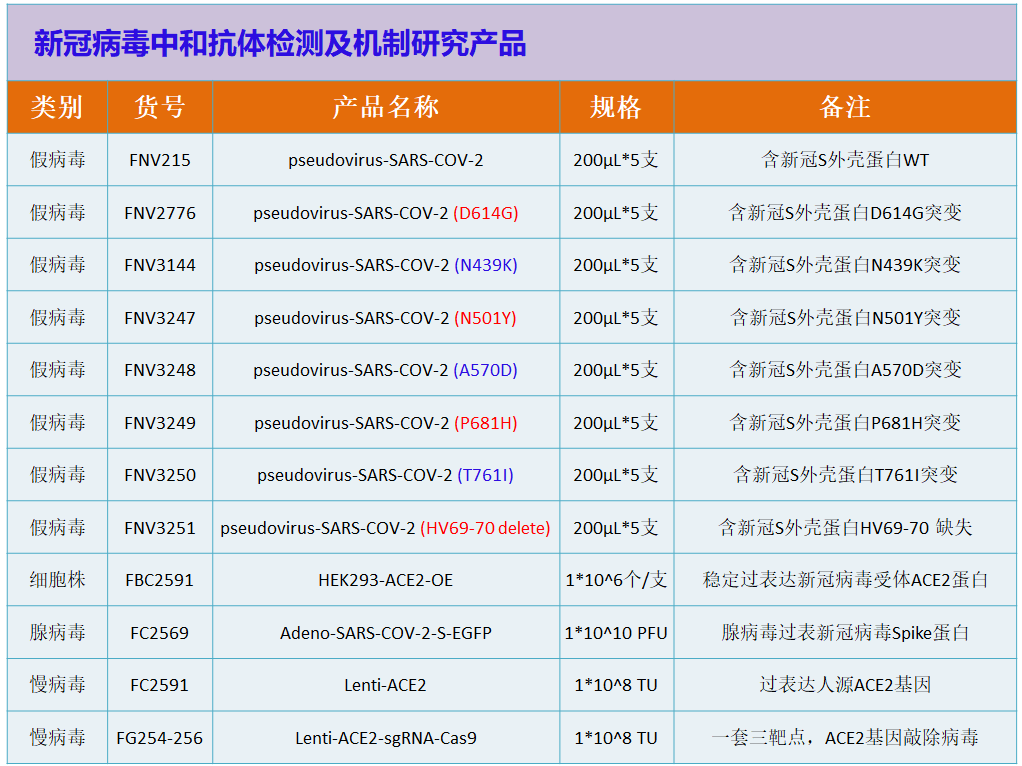
核酸检测假病毒产品