复百澳(苏州)生物医药科技有限公司
9 年
手机商铺
- NaN
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
- 3.7
推荐产品
公司新闻/正文
溶瘤病毒疗法新突破!
2248 人阅读发布时间:2018-12-14 08:17
近日,BoXu等在《Nature biotechnology》(IF:35.724)杂志上发表题为“An oncolytic herpesvirus expressing e-cadherin improves survival in mouse models of glioblastoma”的研究论文,创新的使用了非免疫刺激因子类的基因——CDH1(E-cadhein)与HSV-1TK基因搭配,构建了溶瘤疱疹病毒OV-CDH1,能显著增强溶瘤疱疹病毒对脑胶质瘤的治疗效果,同时可以在治疗效果不确定的情况下,通过“刹车”(HSV-1TK/Acyclovir)对病毒进行杀灭处理,提高了安全性。

CDH1,E-钙粘蛋白
-
由胞外结构域5个钙粘蛋白重复(EC1~EC5),一个跨膜结构域及一个结合p120连环素-和ß-连环素胞的内结构域组成。癌症的发展和转移牵涉了E-钙粘蛋白功能的表达或缺失。
-
肿瘤转移相关性
E-钙粘蛋白表达下调降低了一个组织内细胞黏附的强度,导致细胞活 动性(motility)增加,这可以转而允许癌细胞穿过基底膜入侵周围组织(EMT)发生肿瘤转移。
-
NK细胞杀伤相关性
E钙黏蛋白也是一种粘附分子并且也是KLRG1的配体,而KLRG1是在NK细胞上表达的抑制性受体。
HSV-TK,单纯疱疹病毒胸苷激酶
-
是肿瘤基因治疗研究中常用的自杀基因,可以使一些无毒或低毒的前药转化为强细胞毒性物质,杀死肿瘤细胞。
-
含有HSV-TK的病毒,对疱疹病毒治疗药物Acyclovir非常敏感,更容易被杀灭。
oHSV溶瘤病毒构建
一般来说,oHSV在应用方面有两种主要构建策略:
-
一种是通过缺失或失活一些复制基因,来确保病毒只在增殖的肿瘤细胞中复制,但这也约束了病毒的传播和溶瘤能力;
-
第二种策略是修饰病毒本身介导进入细胞的糖蛋白分子,这种方式保持了病毒的复制和生产能力,但是会降低病毒的感染能力。
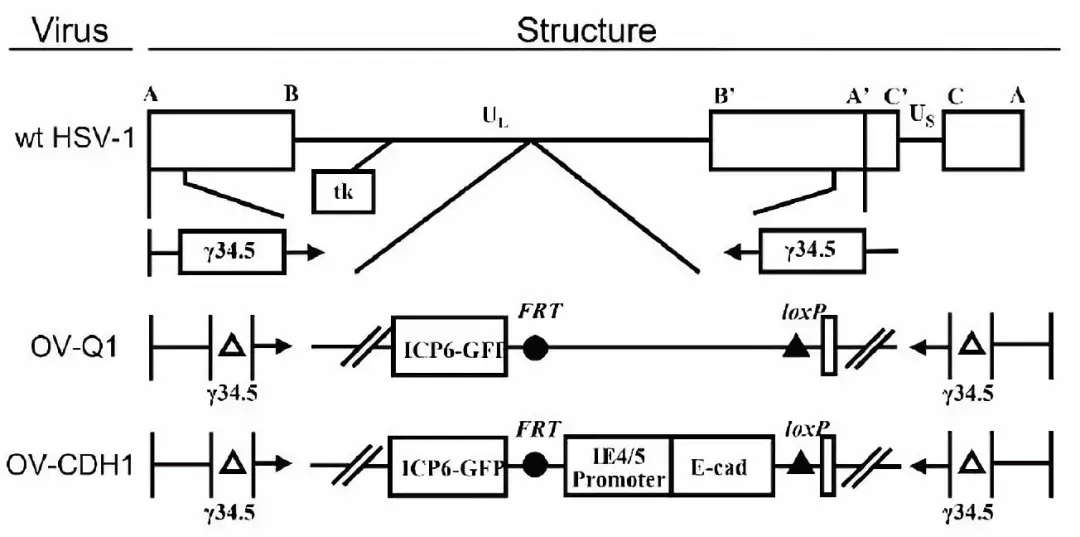
本文作者使用的溶瘤疱疹病毒(oHSV)采用的是第一种构建策略,在删除了ICP34.5区域插入了CDH1基因(E-cadherin),命名为OV-CDH1,而未携带CDH1基因的对照OHSV命名为OV-Q1。
OV-CDH1抑制KLRG+NK细胞杀伤
将感染OV-CDH1的肿瘤细胞与NK细胞进行共培养,发现与OV-Q1相比,感染OV-CDH1细胞被杀伤数量降低。将NK细胞分为KLRG+和KLRG-两个亚群分别进行试验发现时,OV-CDH1感染的细胞可使KLRG+ NK细胞CD107a表达降低,并且使其IFN-γ分泌减少。但在KLRG- NK细胞组中未发现两者的差异。这说明OV-CDH1感染细胞表达的E钙黏蛋白与KLRG+ NK细胞上的KLRG受体结合,抑制了这个NK亚群细胞对病毒性肿瘤细胞的杀伤力。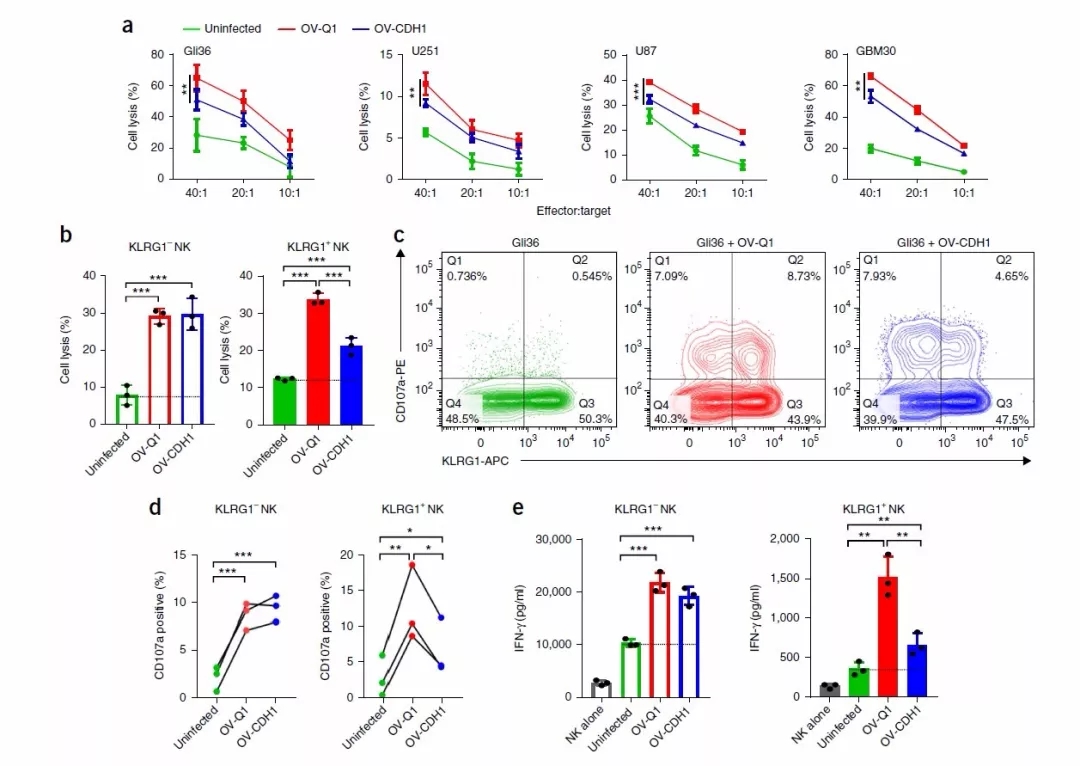
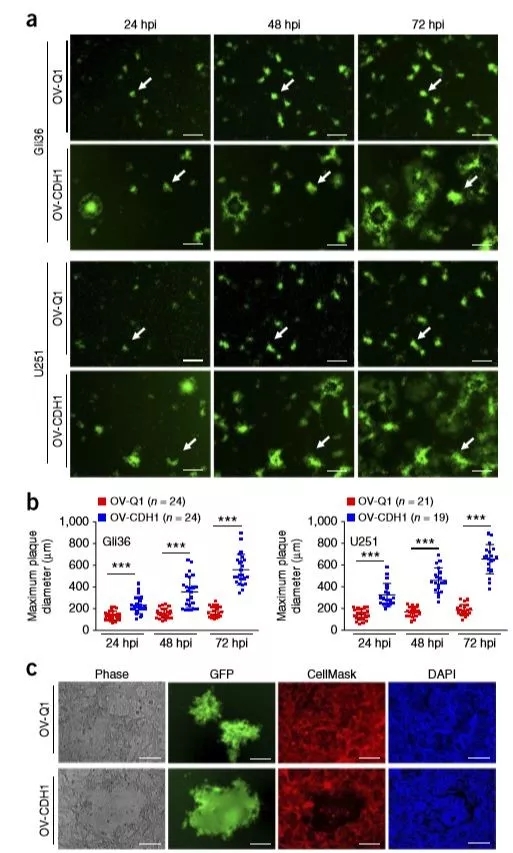
CDH1促进病毒在细胞间的传播
作者评估了OV-CDH1的传播速度,发现OV-CDH1感染的GBM细胞成斑速度较OV-Q1感染的细胞组更快。对细胞斑进一步染色分析,发现OV-Q1感染的细胞呈现单核,细胞之间的膜边界明显,而OV-CDH1感染的细胞呈现多核形态,细胞膜边界不明显,这表明OV-CDH1感染的细胞进行了融合,而这促进了病毒在细胞间的传播,使成斑速度更快。
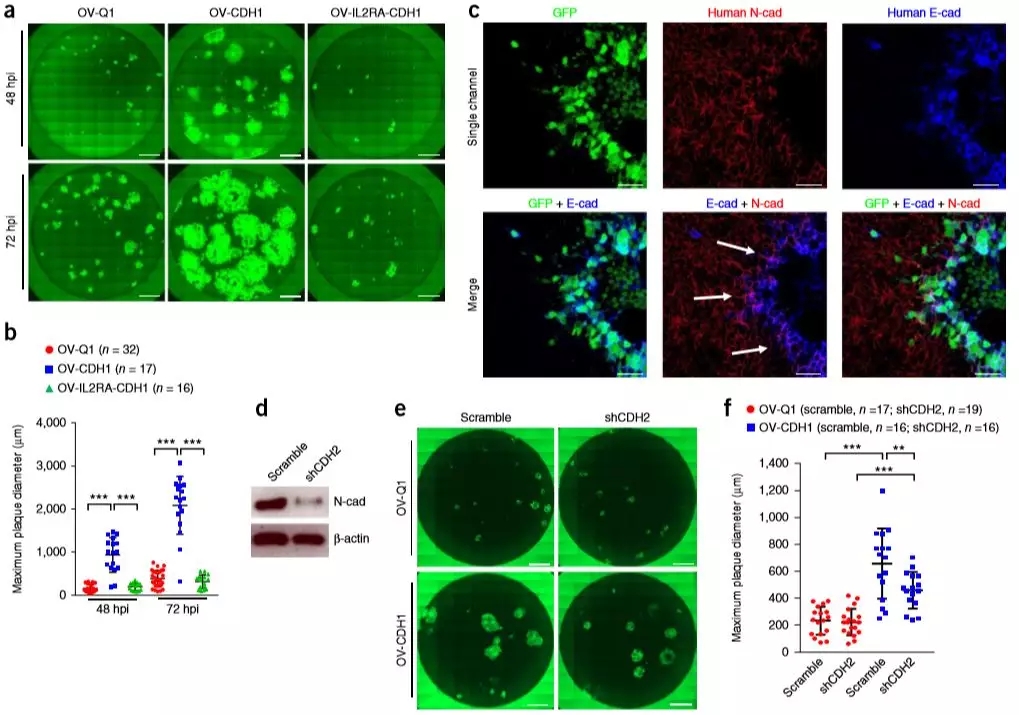
在模仿肿瘤环境的半固相溶液中,成斑实验得到了同样的结果。使用抗体封闭了E钙黏蛋白额胞外区域后,OV-CDH1细胞的成斑效果明显降低,但OV-Q1细胞无明显影响。突变了E钙黏蛋白胞外区域,得到了与抗体封闭同样的效果,这说明E钙黏蛋白的胞外区域对病毒在细胞中的传播起到重要作用,而且GBM细胞自身表达的N钙黏蛋白在这一过程中与E钙黏蛋白结合,不可或缺。
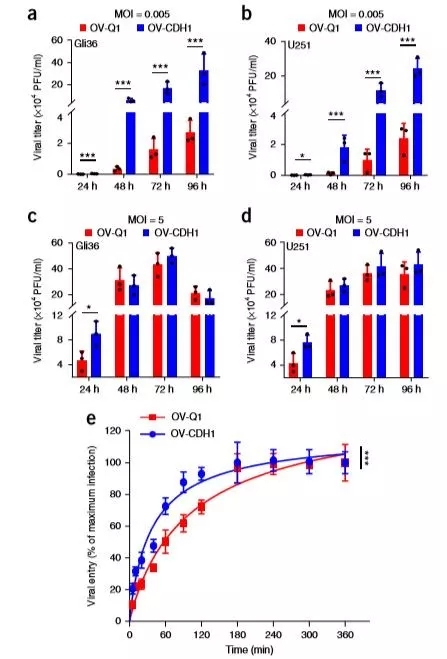
CDH1基因促进病毒感染和增殖
用OV-CDH1和OV-Q1病毒同时在Gli36和U251细胞中进行病毒的扩增复制效率检测,结果显示,含有CDH1基因的OV-CDH1病毒复制效率明显高于无CDH1基因的OV-Q1病毒,且通过动力学分析表明,OV-CDH1病毒对细胞的抓力明显强于OV-Q1病毒,这也间接促进了病毒的传播和病毒的产量。
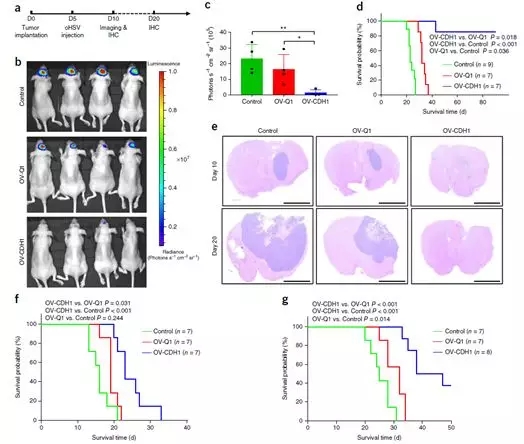
OV-CDH1对脑胶质瘤疗效显著
体外实验获得良好的数据后,作者下一步进行体内验证,在GBM裸鼠异种移植瘤模型中,OV-CDH1显著减低了GBM的肿瘤大小(Control vs. OV-CDH1 **P = 0.009; OV-Q1vs. OV-CDH1 *P = 0.024),并延长了中位生存期(90d vs.34d)。紧接着对免疫完全小鼠进行的Gl261N4(GBM细胞系)移植模型中,与OV-Q1对比,OV-CDH1实验组细胞表面大量表达E钙黏蛋白,形态上表现出了明显的细胞融合现象,和更强的病毒传播能力,中位生存期延长(42.5dvs. 32d)。
刹车机制提升安全性
这种修饰后的溶瘤病毒(OV-CDH1)也存在着安全隐患。如其逃避了NK细胞的追杀,感染OV-CDH1的肿瘤细胞较难被效应细胞清除,以及携带的CDH1会在肿瘤细胞中表达,这其实潜在增强了肿瘤细胞的粘附力等问题。针对这些存在的安全问题,研究者引入了一个“刹车”机制,即OV-Q1和OV-CDH1均携带HSV-1TK基因,使该病毒对acyclovir药物十分敏感,研究者可以根据需要特异性的将其停止。
总的来说,从体内外的最终实验中结果看,过表达CDH1可以显著提升溶瘤病毒对脑胶质瘤的治疗效果。此外,“刹车”机制的引入提高了病毒治疗的安全性,在治疗效果不确定的情况下,可以让病毒药物更加的安全可控。
(更多关于病毒类的文章请关复百澳注公众号)






