复百澳(苏州)生物医药科技有限公司
9 年
手机商铺
- NaN
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
- 3.7
推荐产品
公司新闻/正文
速递|脊髓灰质炎溶瘤病毒临床 I 期,疗效积极!
2007 人阅读发布时间:2021-04-29 14:02
仅供医药专业人士观看
引言:近日,英国期刊《Journal for ImmunoTherapy of Cancer》详细刊载了在 2020 年癌症免疫治疗学会 SITC 年会上公布的有关溶瘤病毒 PVSRIPO 治疗不可切除性黑色素瘤Ⅰ期临床实验结果,总缓解率为 33 %,有 2 例患者观察到病理完全缓解,显示出 PVSRIPO 良好的耐受性、安全性和抗肿瘤活性。

01 临床试验设计
黑色素瘤是一种高度免疫原性肿瘤,部分与高突变相关。此前通过免疫阻断疗法,使用程序化细胞死亡蛋白 1 (PD- 1) 和程序化死亡配体 1 (PD- L1) 的拮抗剂治疗,可以改善一些晚期黑色素瘤患者的预后。但以 PD- 1 为基础的免疫疗法面临原发性、继发性耐药及严重毒害风险的现实问题。
研究者提出了一种有前景的方法,即在肿瘤内给药(溶瘤病毒:PVSRIPO),以促进肿瘤微环境 (TME) 中的抗原呈递,继而恢复或启动抗肿瘤反应,再联合全身 PD- 1 治疗。可能是促进持续抗肿瘤反应的有效策略。
本次临床实验,共有 12 例抗 PD- 1 难治性黑色素瘤患者(IIIB、IIIC 期或 IV 期)入组,治疗方案如下:
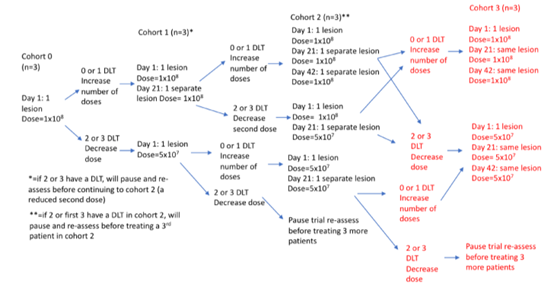
(注射 PVSRIPO 的黑色素瘤患者分组及剂量、治疗周期情况导图)
02 临床试验结果
根据 irRC 标准评估 12 例患者中有 4 例症状缓解,同时观察到 2 例患者的病理完全缓解 (即在注射和非注射病变活检中均未检测到活瘤)。
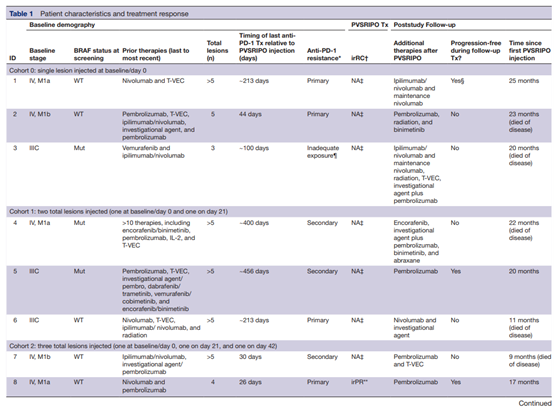
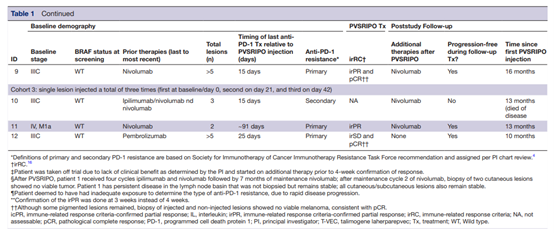
部分病例分析
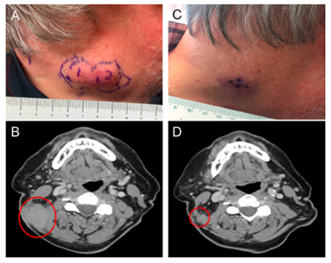
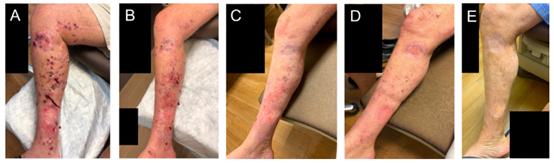
患者 9:该患者表现为右下肢广泛的转移性疾病 (图 3 A),被纳入 2 组,接受了 3 个下肢不同病变部位的 PVSRIPO 注射。第一次注射后 9 天,注射和未注射的病灶均出现了萎缩 (图 3 B)。注射 PVSRIPO 后第 63 天 (图 3 C),对注射病灶和未注射病灶的活检病理分析显示,未检出活肿瘤细胞。首次注射 PVSRIPO 12 个月后,患者有分散、平坦、色素沉着的病灶残留,皆已稳定 (图 3 E)。
患者 11:该患者 PVSRIPO 前肿瘤活检显示有丰富的着色巨噬细胞。这些染色的巨噬细胞可能表明了先前抗 PD- 1 治疗的持续效应。PVSRIPO 会诱导肿瘤相关巨噬细胞的非致死感染。溶瘤病毒治疗可促进 TME 内的免疫反应,这可能克服抗 PD- 1 治疗的耐药性。
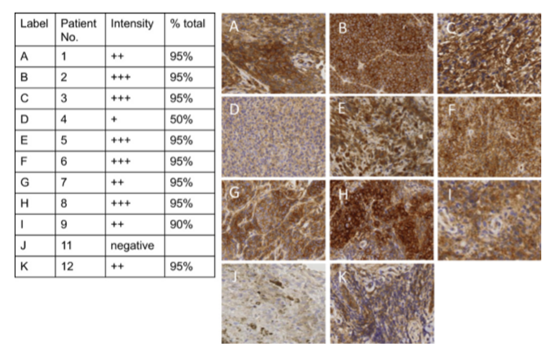
(图为黑色素瘤组织中 CD155 的表达)
临床试验小结
文献来源:Beasley GM, et al. J Immunother Cancer 2021;
延伸拓展
骨髓灰质炎病毒基础生物学特性 骨髓灰质炎病毒(Poliovirus,或称为骨髓灰白质炎病毒)是脊髓灰质炎(小儿麻痹)的病原,又称小儿麻痹病毒。它是一个没有包膜的病毒,由一条单股 RNA 和蛋白质病毒衣壳组成,直径约 25 纳米,属于小核糖核酸病毒科肠道病毒属。
此类病毒具有某些相同的理化生物特征,在电镜下呈球形颗粒相对较小,直径 20~30 nm,呈立体对称 20 面体。病毒颗粒中心为单股正链核糖核酸,外围 60 个衣壳微粒,形成外层衣壳,此种病毒核衣壳体裸露无囊膜。核衣壳含 4 种结构蛋白 VP1、VP3 和由 VP0 分裂而成的 VP2 和 VP4。
-
脊髓灰质炎病毒作用受体
多数病毒侵入细胞需要借助于细胞表面受体,脊髓灰质炎病毒入侵细胞借助的受体为 CD155(也称 nectin-like molecule 5,Necl- 5),该受体是 nectin 样基因家族的重要成员(下表),该家族包含几种细胞表面分子,他们在各种生理学意义上与细胞间黏附功能相关。
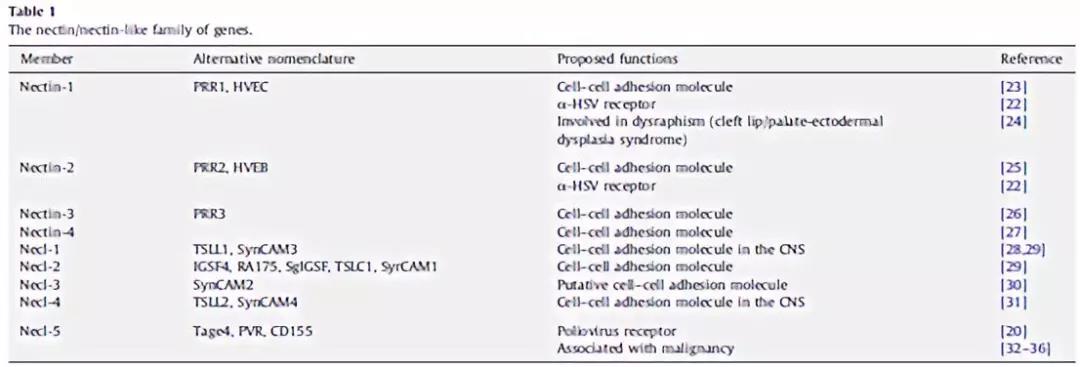
一般来说,受体趋向性或者说非特异性致使溶瘤病毒(OVs)的靶向性受限,限制了溶瘤病毒的研究和临床运用。CD155 分子在恶性肿瘤中广泛上调,而骨髓灰质炎病毒又独特的依赖于 CD155 受体进入宿主细胞,因此,脊髓灰质炎病毒具有成为溶瘤病毒潜力。
利用癌细胞表面上广泛和丰富的分子特征,开发具有天然趋向性的脊髓灰质炎溶瘤病毒是一个非常具有潜力的研究方向!
-
脊髓灰质炎溶瘤病毒对脑胶质瘤的治疗
脊髓灰质炎病毒是一种天然的神经病原体,可以选择性的侵染神经细胞。脊髓灰质炎病毒具有正链 RNA 基因组,其翻译取决于病毒基因组的 5' 非翻译区内的组织特异性内部核糖体进入位点(IRES),其在神经元起源的细胞中有活性并允许翻译没有 5' 帽子的病毒基因组。 Gromeier 等,用鼻病毒 IRES 取代了正常的脊髓灰质炎病毒 IRES,改变了组织特异性。由此产生的 PV1(RIPO)病毒能够选择性地破坏恶性胶质瘤细胞,同时使正常的神经元细胞不受影响。
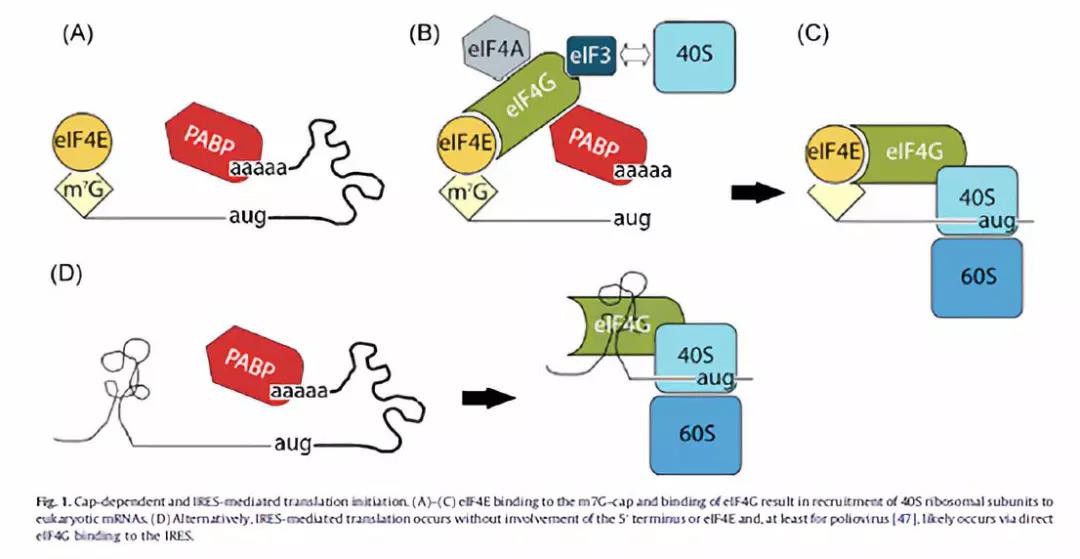
翻译的起始发生在翻译因子 elF4E 与 m7 G 帽子结构的结合(fig1a),并通过结合因子 elF 4 G 将 40 S 核糖体亚基募集至 mRNAs(fig1b)。扫描 5』UTR 使 60 S 亚基在起始密码子和翻译延伸处加入。所以一般来说,因为病毒没有 m 7 G 帽子结构后,病毒不能通过 elF4 G 进行翻译起始。但最近的研究表明,病毒可通过 elF 4 G 与病毒 RNA 的直接相互作用启动病毒蛋白质合成(fig1 d)。
参考资料:
1. Christian Goetz, Matthias Gromeier,Preparing anoncolytic poliovirus recombinant for clinical application againstglioblastoma multiforme.Cytokine & Growth Factor Reviews 21 (2010)197–203;
2. Gromeier M, Lachmann S, Rosenfeld MR, Gutin PH,Wimmer E. Intergeneric poliovirus recombinants for the treatment ofmalignantglioma. Proc Natl Acad Sci USA 2000;97:6803–8;
3. Dobrikova EY, Broadt T, Poiley-Nelson J, Yang X,Soman G, Giardina S, et al. Recombinant oncolytic poliovirus eliminatesglioma in vivo without genetic adaptation to a pathogenic phenotype.Mol Ther 2008;16:1865–72






