复百澳(苏州)生物医药科技有限公司
9 年
手机商铺
- NaN
- 0.7000000000000002
- 1.7000000000000002
- 0.7000000000000002
- 3.7
推荐产品
公司新闻/正文
最新|Nature子刊,COVID-19研究综述及药物研究策略
4337 人阅读发布时间:2020-06-01 10:33

概述部分
迄今为止,尚未批准用于预防或治疗COVID-19的疫苗或有效药物,并且当前的标准护理依赖于支持治疗。介于此,迫切需要开展基础研究,以开发出可以预防和治疗药物。
在这方面,针对COVID-19感染的免疫病理学的治疗方法成为主要焦点。值得注意的是,病毒侵入机体后,产生的系统性免疫是可以在第一时间有效的清除病毒。然而,过度的先天性炎症反应或适应性宿主免疫防御能力受损都,可能导致病毒侵入的组织受损。
多项研究表明,COVID-19患者的先天免疫和适应性免疫均产生了应答,特别是大量的细胞因子和趋化因子释放,即所谓的“细胞因子风暴”,清楚地反映了宿主免疫防御的广泛失控失调。
尽管目前已有针对细胞因子风暴的有效措施,但是由于对COVID-19是触发的免疫信号通路的了解十分有限,对于由其产生的细胞因子风暴的控制,尚需进一步的探索。
鉴于免疫系统在COVID-19中的关键作用,阐明COVID-19病毒作用最相关的基因参与介导病毒感染的生物过程,了解病毒感染过程中细胞信号通路的调控机制,将有助于开发针对相关的靶向分子开展相关的药物研究或疾病治疗。
COVID-19病毒与宿主互作用
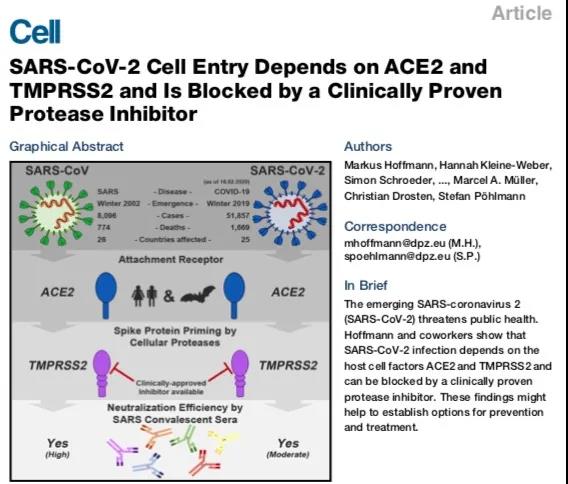
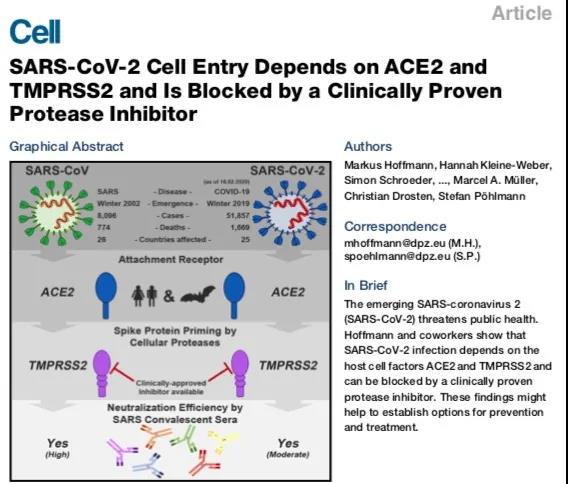
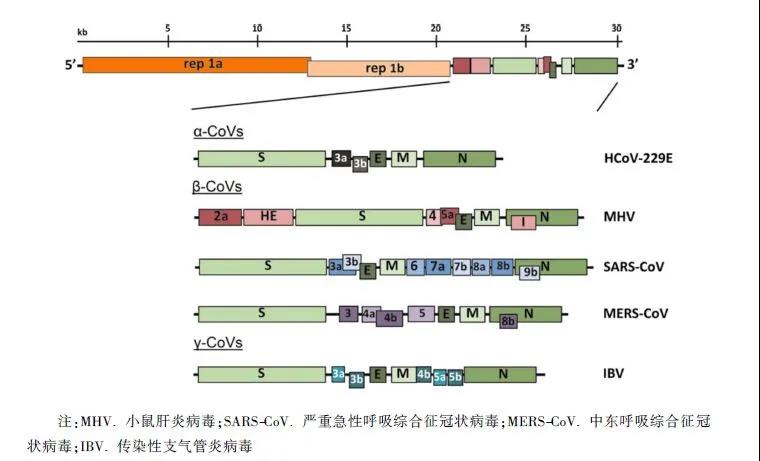
COVID-19是目前发现的可以感染人类的冠状病毒科中的第七个成员,与SARS-CoV和MERS-CoV同属于β冠状病毒。SARS-CoV-2为单股正链RNA,有囊膜,是最大的RNA病毒。
现有的研究,已经揭示COVID-19病毒是通过识别细胞表面的ACE2(血管紧张素转换酶2)受体,内吞的方式进入细胞内。感染的第一步是通过血管紧张素转换酶2(ACE2)受体入侵。其中大多数人体组织,例如口腔粘膜和胃肠道,肾,心脏,血管等均表达ACE2受体。
研究者发现,TMPRSS2在刺突蛋白S1/S2和S2'处切割,启动S蛋白构象改变,膜融合或内吞进入细胞。使用抑制剂 camostat mesylate能够阻断COVID-19病毒入侵。这为靶向设计药物治疗COVID-19提供了思路。但是病毒侵染的细节信息以及潜在的生物学靶标仍有待进一步探究。
研究方案设计
基于COVID-19病毒是通过病毒表面的Spike糖蛋白对细胞表面的ACE2受体的识别,通过内吞的方式进入细胞内。目前,可以通过阻断该过程的发生,扰乱病毒感染细胞的过程,进行疫苗和中和抗体的研发。
新型冠状病毒为高度传染性病毒,出于生物安全性考虑,可以使用假病毒进行相关实验工作。可在保证实验安全的前提下,最大限度的模拟病毒的生物学特性。
-
COVID-19免疫系统病理学
COVID-19病毒进入机体后,会引起其他的抗病毒免疫反应,多数COVID-19患者表现出无症状或轻中度症状(这也是前期不易发现的主要原因),大约15%的患者,表现过度的炎症反应,诱发免疫病理,出现严重的肺炎甚至急性呼吸窘迫综合征,脓毒性休克和多器官衰竭。
重症患者循环B、T、NK细胞减少,单核细胞、嗜酸性/嗜碱性粒细胞也减少,中性粒细胞比例则显著提高,血清中含有高水平促炎因子(包括白介素、趋化因子、集落刺激因子、肿瘤坏死因子)及c反应蛋白、降钙素原等,这些与患者的高死亡率、不良预后直接相关,暗示了免疫反应在病程发展中的作用。
SARS-CoV-2可以影响淋巴细胞的数量和平衡调节宿主适应性免疫,病毒感染导致辅助性T细胞、抑制性T细胞明显减少,初始T细胞则增多,这也促进了炎症的发展。而且记忆T细胞也随之减少,可能意味着存在复发风险。
单细胞RNA测序揭示了B细胞群落发生显著改变,浆细胞显著增加,产生大量SARS-CoV-2特异性抗体,九成患者在20天左右后抗体滴度达到饱和。已有研究表明MERS、SARS可以抑制干扰素介导天然免疫,实现免疫逃逸,同时感染巨噬细胞、T细胞,诱导免疫反应延迟并促进炎症发展,尽管缺乏实验证据,但推测新冠病毒也可能通过类似的机制初期免疫逃逸,后续通过结合其他细胞受体,感染免疫细胞,诱导淋巴细胞死亡从而重塑宿主免疫系统。
抗病毒免疫细胞因子风暴
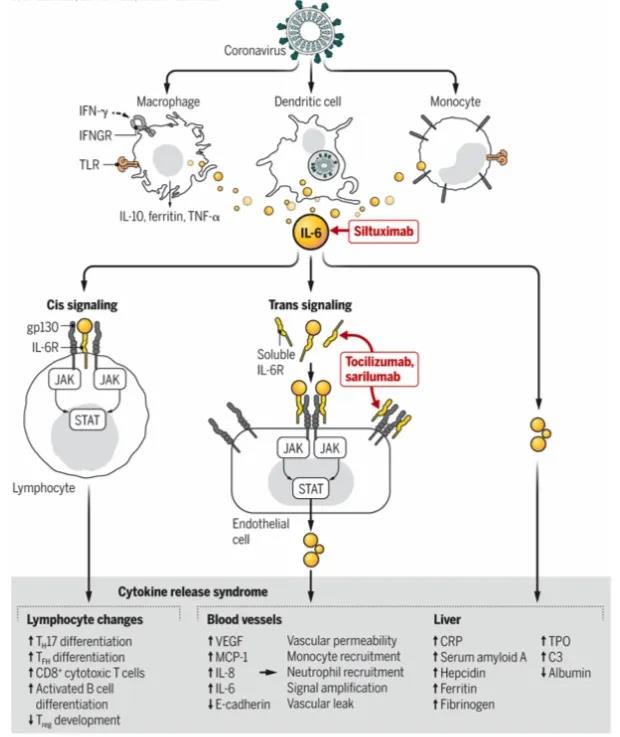
除了病毒直接调节免疫系统,细胞因子风暴在COVID-19病理发展中起到了关键作用。COVID-19细胞因子风暴类似于细胞因子释放综合征和继发性噬血细胞综合征的临床表现,导致血管通透性改变,血浆渗漏以及弥漫性血管凝结,直接危及生命。血浆中的15种细胞因子作为COVID-19生物标志物在重症患者、普通患者及正常人中有明显差异。现有的靶向细胞因子药物可能为COVID-19的治疗提供很大帮助。
肠道微生物
宿主和环境因素导致肠道微生物紊乱,可能诱使正常人易感新冠,瘤胃球菌属、布劳特氏菌属、乳酸菌属等核心微生物丰度与炎性因子呈正相关,代谢组学进一步揭示了氨基酸代谢通路与机体炎症的关系,因此肠道微生物可能通过分泌代谢物诱导个体易感新冠,该过程可以作为潜在的治疗靶标。
信号通路
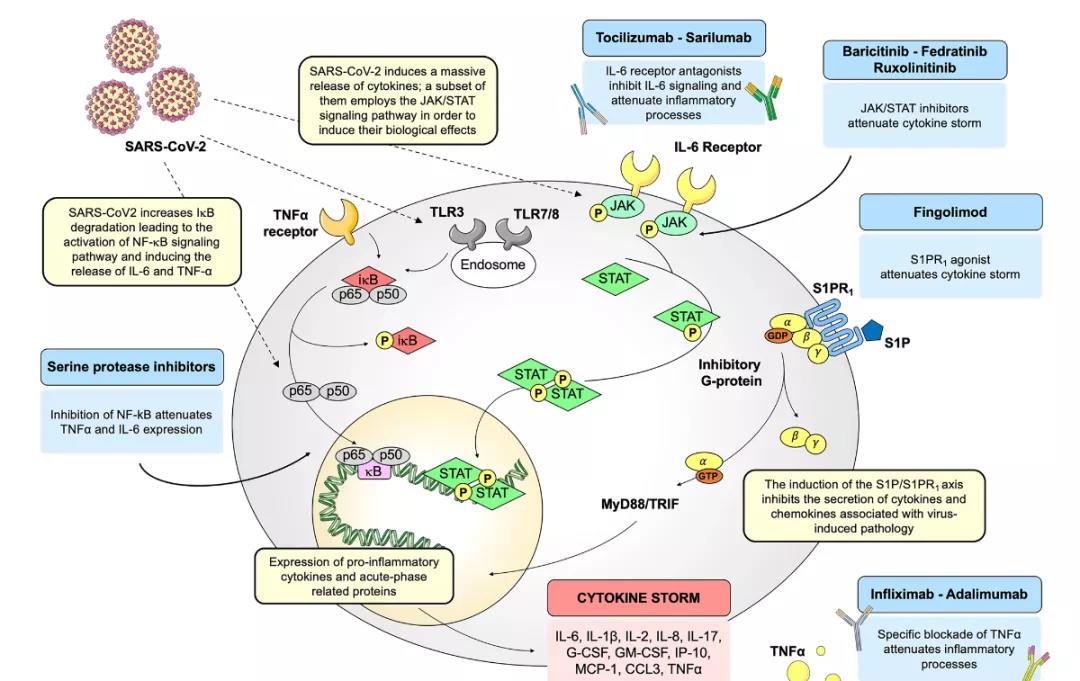
新冠病毒RNA一旦进入细胞内,核酸分子就会被病原模式识别受体,包括内体受体TLR3、TLR7/8,胞浆受体RIG-I/MAD5。天然识别受体激活单核细胞等,进而诱导抗病毒应答和细胞因子产生,激活干扰素、NF-kB、JAK/STAT信号通路。鉴于SARS-CoV-2和SARS的相似性,可能具有相似的细胞内信号通路,因此可以针对这些过程深入探究其分子机制,靶向细胞内分子而非病毒本身,可以有效减弱对病毒的选择压,即使对突变病毒也同样有效。靶向特定信号分子的老药新用可能是候选的治疗药物。
1
NF-kB/TNF-α通路
NF-kB一方面能够激活下游抗病分子与免疫细胞,另一方面组成型表达促进病理性炎症。SARS感染中高水平NF-KB与肺部免疫病理有关,重组S蛋白也能够激活NF-kB信号通路,诱导IL-6、TNF-α表达。动物模型显示老年个体NF-kB活化水平更高,而抑制NF-KB表达可能保护肺部,改善存活率,但是NF-KB抑制剂也会干扰天然免疫抗病通路。相比之下,靶向抑制NF-kB下游的TNF-α具有更小的副作用。而且SARS病毒进入细胞过程中,促进TNF-α转换酶依赖的ACE2受体脱落,因此TNF-α抑制剂具有抑制炎症和抗病毒的双重疗效,仅增加细菌真菌感染风险。事实上,TNF-α单抗在治疗自身免疫病方面已取得成效,有望应用于COVID-19治疗,抑制炎症因子的过度释放。
2
IL-6/JAK/STAT通路
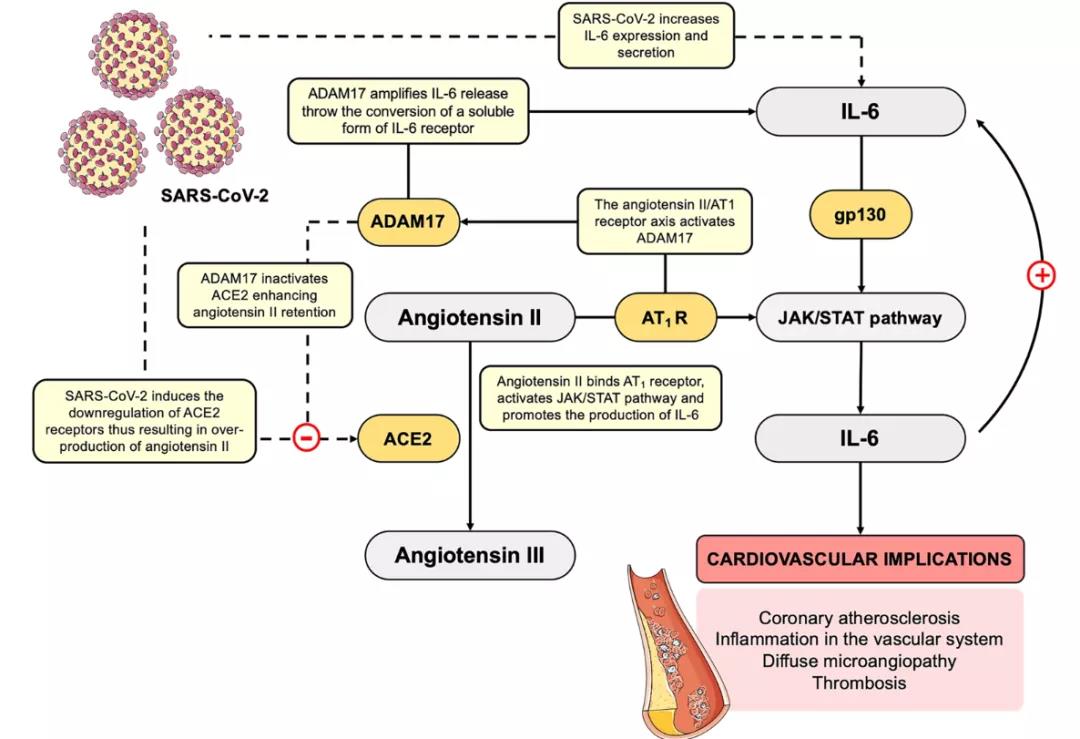
JAK/STAT信号通路是重要的干扰素刺激下游分子,向胞内转导细胞因子等信号,IL-6是JAK/STAT通路重要的激活剂之一,通过gp130受体激活STAT分子,促进细胞因子表达形成正反馈。COVID-19患者中IL-6水平较高,JAK信号通路高度活化,且可作用于不同靶器官,造成相应损伤。此外,IL-6能够与血管紧张素II构成正反馈环路,这一过程受ACE2的抑制,而SARS-CoV-2感染能够促进ACE2下调,加剧IL-6-AngII环路高表达。总体而言,COVID-19能够通过直接或间接的方式诱导IL-6介导的炎症发生。ACE抑制剂和血管紧张素II受体阻滞剂尽管能够抑制该环路,但同时也促进ACE2表达,可能增加新冠感染风险,因此高危人群使用需要谨慎。IL-6抑制剂、JAK抑制剂目前都已开展临床试验,评估在COVID-19治疗中的有效性。
3
鞘氨醇-1-磷酸受体通路
鞘氨醇-1-磷酸作为第二信使,介导免疫细胞功能、炎症发生与组织病变。H1N1流感中S1P能够抑制炎性因子,促进病症缓解。SP1激动剂等靶向SP1通路的药物也具有良好的临床治疗前景。
该文章系统全面地分析了新冠病毒对机体免疫的影响,指出了目前新冠病毒研究的空缺,并提出了合理的假设,有待后续实验的深入探讨,也为目前的疫苗和药物研制提供了新的思考。
COVID-19基因分析与实验设计

冠状病毒的基因组, 单链RNA基因,序列大小约为~30 kb, 具化有5’端的甲基化帽子和3’端的聚腺苷酸尾部。包括多个开放阅读框(ORF)第一个ORF占整个基因组大小的约67%,编码16种非结构蛋白,主要是与病毒复制有关的基因,其他ORF编码辅助蛋白和结构蛋白。 结构形态上类似皇冠,膜表面有三种糖蛋白:刺突糖蛋白(S)、包膜蛋白(E), 膜糖蛋白 (M) 和核衣壳蛋白(N)。
目前,对于COVID-19的研究和药物开发主要集中在两个方向: 1)阻止病毒的进入,如针对病毒Spike蛋白或者细胞ACE2受体的疫苗及中和抗体,多数使用假病毒进行实验; 2)抑制病毒的解旋和复制过程的相关基因。如,木瓜样蛋白酶(PLpro)、3-胰凝乳蛋白酶样蛋白酶(3CLPro)、甲基转移酶(methyltransferase)、RNA依赖的RNA聚合酶(RdRP)以及解旋酶(Helicase)等15~16个蛋白。介于,新冠病毒是RNA病毒的特性,多数采用慢病毒或者假病毒构建相关基因的过表达模型进行相关的机制研究。目前主要的研究病毒基因如下:
-
3CLPro蛋白,ORF1编码,定位于nsp5,位于复制酶基因中心区域,是COVID-19病毒RNA复制时的一个关键蛋白质。
-
PLpro蛋白,ORF1编码,定位于nsp3,和3CLpro共同参与COVID-19病毒RNA的复制,两者对于病毒的活性至关重要。此外,PLpro蛋白参与多种病毒蛋白的前体切割,以形成病毒复制过程中所需的一系列功能蛋白。3CLpro和PLpro是开发抗病毒药物的重要靶点,可抑制病毒复制并降低相关死亡率。
-
-
Helicase解旋酶,ORF1编码,定位于nsp13,是一种利用核苷酸水解的能量将双链核酸分解两条单链。病毒RNA会缠绕起来,研究学者推测其可解开缠绕的RNA链,以便复制或者蛋白翻译。
-
RNA依赖的RNA聚合酶(RdRP),ORF1编码,定位于nsp12,是新冠病毒复制和扩增的关键。一方面以病毒RNA为模板复制子代病毒的基因,另一方面将病毒复制增殖过程中需要的蛋白质和酶的基因转录成mRNA。抗病毒药remdesivir会干扰NSP12。
-
甲基转移酶,ORF1编码,定位于nsp10/nsp16,介导腺苷甲硫氨酸的甲基转移到第一个转录的核苷酸上,参与信号转导、染色体重组和核酸加工等。
-






